【医疗】无关养生
上篇 介绍了药物专利和独占的机制,本篇将以新药研发和制成过程举例说明,药物知识产权的专利保护如何运作。
以下以一间美国药厂A及一个新的合成化学分子药物甲来做例子。
药厂A于2000年研发一个新的化学分子甲(药物甲),觉得有潜能可以开发为新药用来治疗心脏衰竭,于是就在2000年6月向专利局申请专利。若干日子后,专利局倘若批准其申请,将颁发专利公告书,在此例子中,暂且将公告书的日期定为2002年6月。化学分子甲的专利将在2020年6月期满(在《贸易相关的知识产权》(TRIPS)协议之前,专利在2019年6月期满)。得到专利,不意味着化学分子甲一定可以成功推出药物市场售卖。
经过一段时间的研发,包括在实验室及动物身上做试验后(临床前试验),药厂A认为化学分子甲安全及具有治疗潜能,就向美国食品及药物局(FDA)申请批准以开始临床试验。 FDA于2006年6月批准药物甲得以进行临床实验,于是药厂A就必须进行第一、第二及第三阶段的临床试验(简单来说,第三阶段需要的病人试验人数最多,最耗钱和耗时)。时间来到2010年6月,药厂A得到了足够临床试验资料证明药物甲用来治疗心脏衰竭是安全兼有效的,那么它就将这些资料呈上FDA以寻求上市准证。
可再申请延长专利
2012年6月,FDA发出准证让药厂A在医疗市场上销售药物甲,于是药厂A将药物甲命名为“心脏灵”推出,定价一个月300元。由于药厂A觉得官方在审核“心脏灵”的过程中缓慢,导致上市延迟,在《药物价格竞争及专利期限延长法案》 ( HW法案 )的架构下,它可以申请将专利期限延长。
根据此法案,专利期限延长以一次为限,专利延长的年份用一个公式来计算(进行临床试验时间的一半,加上FDA用来审核上市批准的时间——在这个案列里是4年的一半加上2年,因此得以延长4年)。此期限延长最多是5年,而从批准上市的日期到新的专利期限届满不得超过十四年(在此案列里,不得超过2026年6月)。
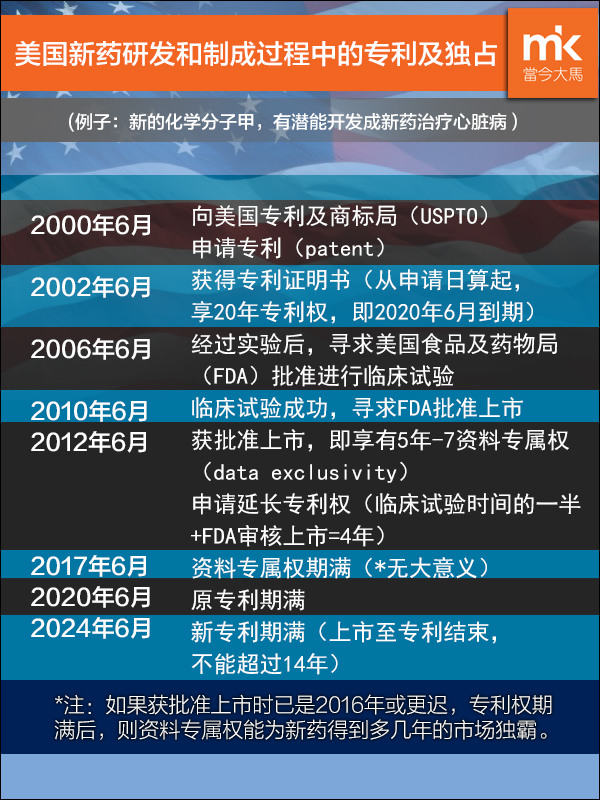 根据HW法案,倘若药物甲是一种新的化学分子,将可享有从被批准上市开始5年的独占(exclusivity)。若是旧的化学分子,但用来开拓新的疗法或疾病,可享有3年的独占。另一个级别是孤儿药品(orphan drug),即是用来治疗罕见疾病的药物,则将在美国市场享有FDA颁发的7年独占期限(孤儿药品在欧盟及日本享有10年的独占期),这些独占权大多数是资料专属权(data exclusivity)。如果药厂A进行“心脏灵”在儿童群体疗效的研究,那么它就可以再获得6个月的专利及独占期延长。
根据HW法案,倘若药物甲是一种新的化学分子,将可享有从被批准上市开始5年的独占(exclusivity)。若是旧的化学分子,但用来开拓新的疗法或疾病,可享有3年的独占。另一个级别是孤儿药品(orphan drug),即是用来治疗罕见疾病的药物,则将在美国市场享有FDA颁发的7年独占期限(孤儿药品在欧盟及日本享有10年的独占期),这些独占权大多数是资料专属权(data exclusivity)。如果药厂A进行“心脏灵”在儿童群体疗效的研究,那么它就可以再获得6个月的专利及独占期延长。
专利药上市至独占期限
以上的例子里,“心脏灵”是专利药(patent drug),药物在2012年6月上市,新的专利有效日期是2024年6月(最初获得的专利期限到2020年6月),因此 “心脏灵”从开始上市到专利期限届满,有12年的时间在独霸市场里售卖。若有儿童病患的临床试验资料,它因为拥有专利而得以独霸市场的期限将延长至12年6个月。
在此个案中,“心脏灵”是新的化学分子,因此它在美国的独占期将在2017年6月届满(从上市开始5年),那时候其专利还有5年才届满。由于独占期限和专利期限并不是附加(additive)的,因此“心脏灵”的独占期限并非是好像有些人认为的20(专利)+4(专利延长四年)+5(独占),总共29年。在此个案中,“心脏灵”从上市到学名药(仿制药)可以进入市场,专利药有效独霸市场的期限其实最长是12年6个月(倘若独占期限和专利期限是附加的,那么它从上市开始独霸市场的期限是17年6个月)。
绝大多数时候,由于新化学分子申请专利的程序(申请专利的时候,通常不会知道此分子最终的功效),加上要证明药物安全及具有疗效的冗长过程,从药物开始在市场售卖到独霸期限结束,几乎肯定不会超过20年。
以美国来说,在现有的法律架构下,即使得到专利期限延长,也不会超过14年,再加上因为儿童试验的6个月延长,至多是14年6个月。在一些情况下,由于药物开发到临床试验的完成太过冗长,可能会发生当药物得到FDA许可上市时,本来的专利期限已经寥寥无几,甚至已经过期。在这种情况下,独占权将让此药物得到5年至7年的市场独霸。
抗癌药物“格列卫”之例
 回到上篇讨论的药物,格列卫(Glivec,在美国被称为Gleevec)肯定是抗癌历史上最为成功的药物,奇迹般改变了本来只有三五年寿命病患的命运,让他们恢复健康。许多服用格列卫的病患已经很好的存活超过十个年头,完成学业及成家立业,也投入社会成为建设国家劳动力的一份子。
回到上篇讨论的药物,格列卫(Glivec,在美国被称为Gleevec)肯定是抗癌历史上最为成功的药物,奇迹般改变了本来只有三五年寿命病患的命运,让他们恢复健康。许多服用格列卫的病患已经很好的存活超过十个年头,完成学业及成家立业,也投入社会成为建设国家劳动力的一份子。
这个药物背后的金钱代价有多大?在马来西亚,市场价格大约是一年10万令吉。迄今在马来西亚公立医院系统下有超过1千名慢性粒性白血病(Chronic Myeloid Leukemia,CML)病患服用格列卫,若用市价计算至少是每年1亿令吉的药物费用。
卫生部在2016年财政预算案里获得230亿令吉拨款,一般上药物开支占了大约15%,就是35亿——若是以市价来买药提供给患者,每100令吉的药物支出,就要用2.9令吉来支付格列卫,这明显是不可能负担得起的(注1)。专家估计全球只有3成的CML病患能够获取格列卫,许多原因造成这个悲剧,药物价格昂贵当然是其中一个 主因 。
格列卫的化学成分于1993年在多个国家注册专利,虽然后来药厂改进分子后再追加专利,在多数国家它的原始分子的专利在2013年结束。加拿大没有延长专利期限的法律,而8年的独占期限也已经在2009年结束(6年资料专属权加上2年市场专卖权),因此在2013年开始生产伊马替尼(Imatinib,格列卫的化学成分)的学名药。
印度生产格列卫的学名药
印度则是在早几年已经开始生产及发售伊马替尼的学名药,诺华大药厂2013年在印度打输了格列卫的专利官司,纽约时报 估计 印度生产的学名药价格(一年2500美元)是专利药的3.6%,该报是以美国药价一年7万美元来计算。
事实上,格列卫在美国的价钱是一年9万2千美元,所以印度的学名药价格其实只有专利药的2.7%,如此推算,为一个病患购买专利药,同样的花费可以用学名药来医治36个CML病患。注意学名药的价格,即使是一年2500美金,在印度绝大多数人依然负担不起,换成马币计算,价格是每年1万令吉,对许多马来西亚人来说依然是个奢侈的价码。
伊马替尼在美国的原始专利本来也在2013年5月28日年结束,在HW法案法案下,药厂取得586天的专利 延长期限 ,加上因为在儿童群体的试验得到的6个月延长,专利权在2015年7月4日结束(FDA颁发的资料专属和市场专卖期限此时已经过期)。药厂在法律允许的架构下总共多获取了766天的独占权。
总部设于印度的太阳制药公司本来已经得到FDA批准将学名药上市,诺华大药厂提出诉讼(大药厂惯用来延迟学名药上市的手段之一),后来在2015年5月和太阳制药公司和解,将学名药的上市日期推迟至2016年2月1日,双方都将此项和解的条件内容保密。结果格列卫在美国总共多得到大约2年半的独占期。
企业用法律灰色地带牟利
格列卫全球销售额是47亿美元,单在美国市场就销售了25亿美元,2年半在美国的延长市场独占换成的金额是63亿美元(63亿美元是世界银行估计马来西亚2014年GDP的2%)。 HW法案的精神其实是要降低学名药进入市场的门槛,吸引竞争以便降低药价,然而一些企业利用法律灰色地带钻空子,造成了社会学里所谓的非预期性后果(unintended consequences)。
格列卫学名药明年将在美国及欧洲入场,会如何影响全球治疗CML,甚至对抗癌症的方针和走向,还是一个未知数。接下来的学名药和专利药之争,将继而把战场扩大到如何让贫穷及发展中国家的病患获取药物,无可避免的会牵涉到跨国企业、自由贸易协定等等的矛盾与争议。药品与医疗供给及获取的斗争已经不只是医疗界的家事,医疗对人类的重要及将要崩坏的风险,无可避免的会将每个人都拉进这场战斗。
 TRIPS协议里的资料专属权没有将化学分子药物和生物制剂(biologic medical product,或biologics)分开,TPPA则是特别定义生物制剂,让其和化学分药物子一样要有资料专属权,除此以外,基本上各国现有的其他药品专利和独占的架构并没有变动。在TPPA协议未公开之前,有些团体指控泄漏的协议带有延长专利的条文,从现在已经公开的TPPA内容我们可以得出结论,即使得到5年或8年的独占期,生物制剂也不太可能享有超过14年的市场独霸期限,意味着现今的游戏规则没有重大的改变。
TRIPS协议里的资料专属权没有将化学分子药物和生物制剂(biologic medical product,或biologics)分开,TPPA则是特别定义生物制剂,让其和化学分药物子一样要有资料专属权,除此以外,基本上各国现有的其他药品专利和独占的架构并没有变动。在TPPA协议未公开之前,有些团体指控泄漏的协议带有延长专利的条文,从现在已经公开的TPPA内容我们可以得出结论,即使得到5年或8年的独占期,生物制剂也不太可能享有超过14年的市场独霸期限,意味着现今的游戏规则没有重大的改变。
生物制剂和化学分子虽然都是药品,但它们有明显的不同。生物制剂的专利有特定的挑战点,所以有些人认为独占权需要订得比较长,但同时生物相似药品进入市场的门槛不低,很难以化学分子的学名药拿来做典范。至于生物制剂其他方面的课题,则不在本篇详细讨论。
反TPPA者未充分了解专利
全球药物及医疗获取的不公,当然需要获得正视,也需要当权者有决心设法解决问题。摆脱专利和独占是否就是答案及解决这个问题的特效秘方?这一点其实还存有许多灰色地带。今天我们看到很多反对TPPA的个人和团体都以发展中国家的药物获取障碍当作主打,然而许多人对专利及独占没有充分的了解,以致问题的症结没有被整理出来研讨,却瞄准错误目标(例如 声称 独占时期是20+5年,总共是25年),浪费了舆论的篇幅,也导致失去了教育公众思考医疗难题的机会。
从WTO到TPPA,知识产权——尤其是关于医疗的知识产权保护——就一直是全球的争议和拉锯战。现今非政府组织、团体及个人对TPPA协议内医疗可能加强垄断及限制发展中国家获取药物的抗议,并非前无古人。人目短于自见,故借镜以观形。下一篇,我们将讨论25年前爱滋病活动团体及第三世界国家在TRIPS的法律架构及企业垄断药物销售的背景下,展开抗议活动的故事。
注1 :马来西亚的格列卫及第二代CML药物供应有一个由卫生部、企业、国际与本地非政府组织及医师参与的特别药物获取计划,在此不详细论述,资料可看 此处 。
【延伸阅读】
翁诗钻毕业于马大医学系,和死神拔河第十九个年头,深感生命朝夕无常,对医学没有幻想,只能脚踏实地赚一份薪水。但愿以后墓志铭上刻的是——一个曾经医治过人类的人。
本文内容是作者个人观点,不代表《当今大马》立场。

